界面新聞記者 | 李科文
界面新聞編輯 | 謝欣
界面新聞注意到,10月21日,百利天恒港交所IPO申請通過聆訊,即將在港股二次上市。
10月22日,百利天恒向界面新聞表示,港股上市是百利天恒國際化戰略中的關鍵一步,將為公司拓展國際融資渠道,快速推進創新研發管線的全球性臨床試驗以及未來全球商業化,助力公司成為在腫瘤領域保持全球領先地位的跨國藥企。
從此次募資用途來看,百利天恒已展露出全球化的野心。
一方面,百利天恒計劃在美國開展多項在研藥物的臨床試驗,推動核心管線邁入國際驗證階段。另一方面,考慮到在海外尚未有生產基地,百利天恒也計劃通過自建或收購的方式,建立境外生產基地,實現全球范圍內的研發與生產協同。
自2023年12月與跨國藥企百時美施貴寶(BMS)就抗體偶聯藥物(ADC)Iza-bren(項目代碼:BL-B01D1)達成總價84億美元的合作以來,隨著Iza-bren臨床數據的持續驗證,該藥已被視為繼PD-(L)1后下一代潛在基石療法,百利天恒始終處于行業聚光燈之下。

其管線是否足以支撐全球化野心,需要市場一步步驗證。
截至2025年10月,百利天恒共擁有15款處于臨床階段的創新藥物,另有2款候選藥物已獲IND受理。其中,已有6款產品在美國啟動臨床試驗。

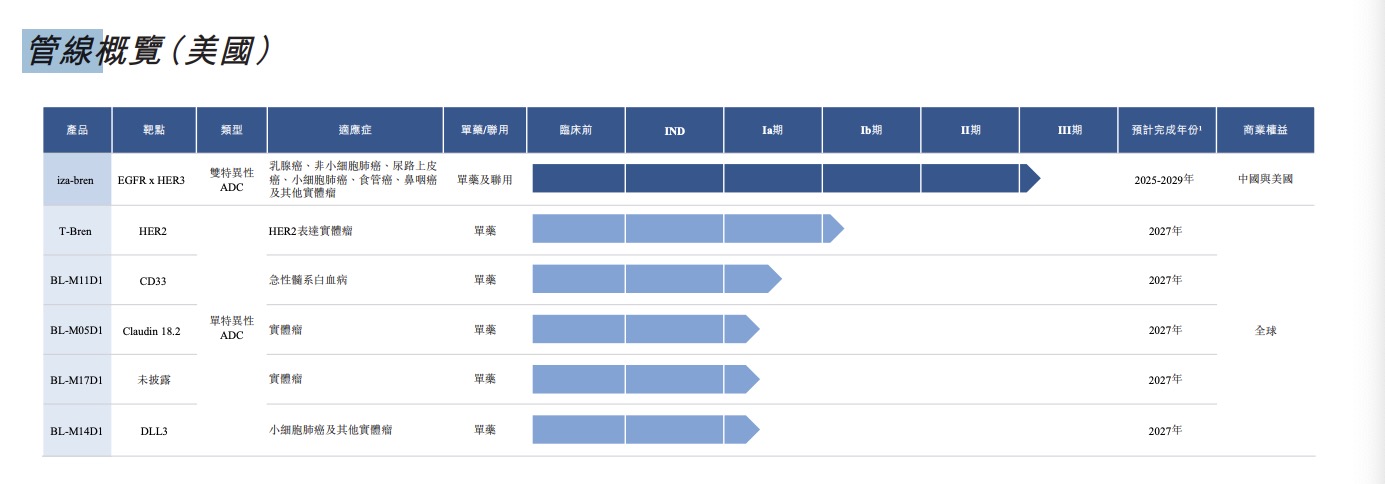
其中,最為核心的是百利天恒的創新藥轉型之作Iza-bren。
Iza-bren(BL-B01D1)是一款靶向EGFR與HER3的雙特異性抗體偶聯藥物(ADC),是目前全球首個、也是唯一一個進入III期臨床階段的雙抗ADC品種,具備高度差異化的技術路徑和臨床價值。
Iza-bren 在研適應癥覆蓋范圍非常廣泛,包括肺癌、乳腺癌、頭頸鱗癌、鼻咽癌、食管癌、胃癌、結直腸癌、膽道癌、尿路上皮癌和卵巢癌等多個瘤種,且目前已累計有7項適應癥被CDE納入突破性治療品種名單,并有1項適應癥被美國FDA授予突破性療法認定
這款明星產品自2023年12月與百時美施貴寶達成高達84億美元的全球合作協議以來,持續受到市場關注。
在2025年歐洲腫瘤內科學會(ESMO)年會,Iza-bren跨人群、跨瘤種的廣譜特性得到進一步驗證。
百利天恒在ESMO大會上公布了Iza-bren針對西方人群的實體瘤研究數據。
該研究覆蓋年齡更大(中位年齡65歲)、接受過三線及以上治療的57.9%患者群體,展現了Iza-bren跨人群和跨瘤種的普適性療效。
在晚期重度經治多種實體瘤患者中,其總體客觀緩解率(cORR)高達55%,中位無進展生存期(mPFS)達到5.4個月。
Iza-bren尤其在肺癌和乳腺癌中觀察到強勁積極信號:EGFR野生型非小細胞肺癌(NSCLC)的cORR達到75%,疾病控制率(DCR)為100%;乳腺癌的cORR更是高達100%。
作為目前全球首個針對西方人群展開的大樣本、多瘤種雙抗ADC研究,Iza-bren的最新數據不僅延續了國內早期研究中的優異表現,在療效和人群適配性上更進一步強化了其“下一代基石療法”的潛力。
業內普遍將 Iza-bren 視為最具潛力挑戰“藥王”帕博利珠單抗地位的下一代基石腫瘤療法。
據經濟觀察網,百利天恒董事長朱義預測Iza-bren潛在的年銷售峰值200億美元。參考帕博利珠單抗(Keytruda)2024年295億美元的全球年銷售額,界面新聞以200億美元的峰值銷售倍數法進行對標估算。
在設定估值倍數為3倍(適用于長專利期、高毛利、強護城河的創新藥品類),并給予50%的綜合成功概率后,Iza-bren的管線估值天花板預估達300億美元(折合人民幣約2136億元)。
除了Iza-bren,T-Bren是百利天恒在ADC領域布局中的另一個關鍵支點。
作為一款靶向HER2的抗體偶聯藥物,百利天恒稱,T-Bren具備同類最優(Best-in-class)的潛力。
截至目前,T-Bren正于中美同步推進14項臨床試驗,包括6項為關鍵性注冊研究、2項處于II期、3項處于I/II期、3項處于I期的臨床實驗。
T-Bren也是百利天恒本輪融資中最優先投入的方向。
T-Bren的對標品種是由第一三共與阿斯利康聯合開發的HER2 ADC藥物德曲妥珠單抗(Enhertu)。
據智慧芽數據,2024年德曲妥珠單抗在中國市場的銷售額為93億日元(約合人民幣4.32億元),但全球銷售額則高達5243億日元(約人民幣246億元),同比增長52.5%,其中主要收入來自美國、歐洲及日本等成熟市場。
從德曲妥珠單抗的全球銷售結構來看,不難理解百利天恒出海的急迫心理。T-Bren能否復制德曲妥珠單抗國際商業成功,并最終超越,將直接決定百利天恒是否有第二增長曲線。出海是更曠闊的市場。
界面新聞了解到,百利天恒已于2024年2月啟動T-Bren在美國的首個I期臨床試驗,旨在評估其在HER2表達晚期實體瘤中的安全性與初步療效。若I期結果積極,百利天恒將計劃啟動III期關鍵研究,優先布局乳腺癌與胃癌等適應癥,并以此作為向FDA遞交生物制品許可申請(BLA)的基礎。
除了Iza-bren與T-Bren,百利天恒還想推動多個ADC與多特異性抗體管線的全球化布局。
在ADC平臺方面,百利天恒正同步推動多款臨床及臨床前候選藥物的全球進展。
BL-M08D1為一款自主開發的單特異性ADC,計劃于2025年向FDA遞交IND申請,并在獲批后一年內,啟動其在多種實體瘤適應癥中的I期臨床試驗;BL-M17D1則采用百利天恒自有平臺設計的新一代有效載荷結構,已在美國進入I期臨床階段,預計2027年完成數據收集;此外,百利天恒還同步推進BL-M11D1、BL-M05D1、BL-M14D1等多個ADC分子在美國的早期臨床試驗,同樣預計在2027年前后形成初步臨床讀數。
在多特異性抗體方向,百利天恒依托GNC平臺,也開發多個具備差異化機制的創新分子。
GNC-077在體內研究中已展現出對多種實體瘤的強效抑制能力;GNC-038則是一款用于血液腫瘤及自身免疫疾病治療的四特異性抗體,目前正推進臨床研發;GNC-035、GNC-039等第一代候選藥物,以及新一代GNC分子的臨床前開發與驗證也在推進。
此外,HIRE-ARC(抗體-藥物偶聯環狀肽)平臺,百利天恒也已啟動針對BLARC001等候選藥物的臨床試驗,探索ARC分子在多瘤種治療中的應用潛力。



