界面新聞記者 | 陳楊
界面新聞編輯 | 謝欣
繼禮來減肥藥替爾泊肽之后,信達生物的國產(chǎn)減肥藥瑪仕度肽也“頭對頭”戰(zhàn)勝了司美格魯肽。
界面新聞注意到,10月27日,信達生物公布瑪仕度肽與司美格魯肽的頭對頭III期臨床研究(DREAMS-3,NCT06184568)結(jié)果。在中國2型糖尿病合并肥胖受試者中,接受治療第32周時,瑪仕度肽組HbA1c(糖化血紅蛋白)<7.0%且體重較基線下降≥10%的受試者比例為48.0%,優(yōu)效于司美格魯肽組的21.0%(P值<0.0001),達到該研究的主要終點。
也就是說,該研究中,對于中國2型糖尿病合并肥胖患者,瑪仕度肽在血糖控制和體重管理的綜合療效上顯著優(yōu)于司美格魯肽。
另外,第32周時,瑪仕度肽組和司美格魯肽組HbA1c較基線變化均值分別為?2.03%和?1.84%,體重較基線平均百分比降幅分別為10.29%和6.00%(P值均<0.05)。研究期間,瑪仕度肽整體安全性特征與既往臨床研究一致,未發(fā)現(xiàn)新增安全性信號。胃腸道不良反應(yīng)是最常見的不良事件,多為輕度或中度。
這其中,司美格魯肽為諾和諾德的GLP-1受體激動劑,替爾泊肽和瑪仕度肽分別為GIP/GLP-1、GCG/GLP-1雙受體激動劑。這三款藥物均為各自靶點上全球首個獲批的周制劑,三者的2型糖尿病和減重這兩個最主流適應(yīng)證也均已在國內(nèi)獲批。

信達生物還提到,DREAMS-3是全球首個在糖尿病治療領(lǐng)域GCG/GLP-1雙受體激動劑與司美格魯肽開展頭對頭比較的III期臨床研究。
具體而言,該研究是一項多中心、隨機、開放標(biāo)簽III期臨床試驗,共入組349例受試者。入組對象為經(jīng)單純飲食運動干預(yù)伴/不伴二甲雙胍單藥治療血糖、體重控制不佳的中國早期2型糖尿病(病程<10年)合并肥胖受試者。
受試者平均年齡42.4歲,平均病程1.8年,平均基線HbA1c為8.02%,平均基線體重為90.47kg,平均基線BMI為32.98kg/m2,以1:1比例隨機接受瑪仕度肽6mg或司美格魯肽1mg治療32周(常規(guī)治療期)。
界面新聞注意到,除與司美格魯肽“頭對頭”外,高劑量瑪仕度肽也在開展與替爾泊肽頭對頭治療中重度肥胖的臨床試驗。
GLP-1類降糖減重藥物是目前海內(nèi)外最熱門的研發(fā)領(lǐng)域之一。
據(jù)經(jīng)濟學(xué)人報道,預(yù)計到2031年,全球GLP-1多肽類藥物銷售規(guī)模有望達1650億美元,美國市場可達1000億美元,其中減重適應(yīng)證市場將超過糖尿病市場,占到六成。
除前述三款藥物外,界面新聞曾報道,國內(nèi)已有近10款司美格魯肽類似藥處于上市申請階段。
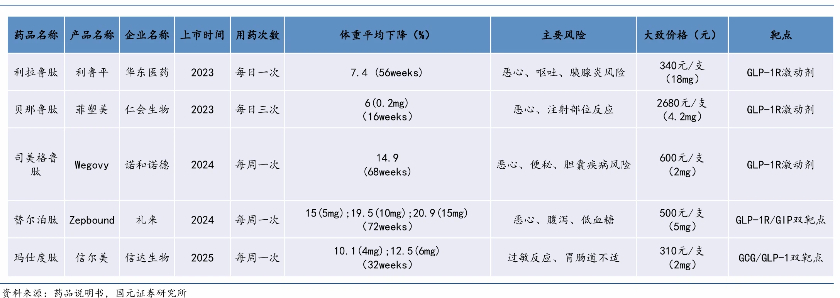
由此,未來GLP-1類藥物的差異化設(shè)計成為各家重要的競爭方向。
10月26日,界面新聞從第十屆醫(yī)藥創(chuàng)新與投資大會上獲悉,多個GLP-1類藥物臨床研究的主要研究者、北京大學(xué)人民醫(yī)院紀立農(nóng)教授提到,新一代減重藥物的開發(fā)策略包括多靶點激動劑、胰淀素(Amylin)與GIP通路(與GLP-1聯(lián)用)、偏向性(Biased)GLP-1激動劑、肌肉保護策略、改善依從性等。

另外,紀立農(nóng)表示,(當(dāng)下)針對肥胖的治療體系剛剛起始,和四十年前的糖尿病差不多。實際上從司美格魯肽上市后,業(yè)界才突然對這個領(lǐng)域的藥物開發(fā)和長期的疾病管理感興趣,(因此)今后的路還非常長。
前述會議上,恒瑞醫(yī)藥臨床研發(fā)醫(yī)學(xué)高級總監(jiān)陳虹亦提到數(shù)個減重未滿足的臨床需求與未來關(guān)注趨勢,例如肥胖常伴隨糖尿病、心血管疾病等,如何實現(xiàn)代謝全面管理;繼發(fā)性肥胖需針對病因治療,現(xiàn)有藥物尚無法覆蓋,青少年、老年人肥胖仍缺乏安全有效的干預(yù)手段,如何覆蓋更廣泛人群。



